Đình chỉ lưu hành và thu hồi loại thuốc tim mạch, huyết áp
Cụ thể, thuốc viên nén bị đình chỉ lưu hành, thu hồi có tên Miratel 40 (Telmisartan 40mg), số lô 16: MIV05; HD: 05/02/2018, SDK: VN-12172-11 do Công ty Miracle Labs (P) Ltd. (India) sản xuất, Công ty Cổ phần xuất nhập khẩu y tế Thành phố Hồ Chí Minh (Yteco) nhập khẩu.
Theo Cục Quản lý Dược, nguyên nhân thu hồi loại thuốc này là do không đạt chất lượng về các chỉ tiêu khối lượng trung bình viên và độ hòa tan.
Trước đó, mẫu thuốc này đã được Viện Kiểm nghiệm thuốc Thành phố Hồ Chí Minh lấy tại Công ty TNHH Dược phẩm Huy Thông, gian 7, 344 Tô Hiến Thành, P.14, Quận 10, Thành phố Hồ Chí Minh để kiểm nghiệm.
Cục Quản lý Dược đã gửi thông báo đình chỉ lưu hành, thu hồi loại thuốc này tới các Sở Y tế trên toàn quốc. Cơ quan này cũng yêu cầu Công ty Cổ phần xuất nhập khẩu y tế Thành phố Hồ Chí Minh (Yteco) phải phối hợp với nhà cung cấp và phân phối khẩn trương gửi thông báo thu hồi của Cục đến các địa điểm phân phối và sử dụng thuốc viên nén Miratel 40 (Telmisartan 40mg) thuộc số lô trên và tiến hành thu hồi toàn bộ lô thuốc này.
Cục Quản lý Dược yêu cầu Công ty Cổ phần xuất nhập khẩu y tế Thành phố Hồ Chí Minh phải gửi báo cáo thu hồi về Cục Quản lý Dược trước ngày 13/2/2017, hồ sơ thu hồi bao gồm số lượng nhập khẩu, ngày nhập khẩu, số lượng thu hồi, các bằng chứng về việc thực hiện thu hồi tại các cơ sở bán buôn, bán lẻ, sử dụng đã mua thuốc.
Tin mới hơn

Bộ Y tế chỉ đạo khẩn sau ca mắc cúm gia cầm A(H9) trên người đầu tiên

Bộ Y tế yêu cầu tăng cường kiểm tra, giám sát kê đơn thuốc
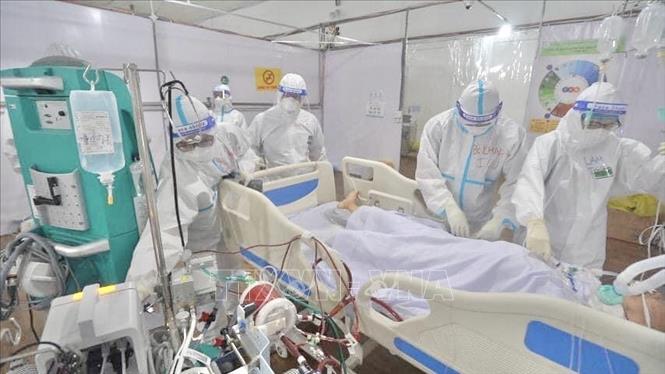
Ngày Thầy thuốc Việt Nam 27/2: Ra mắt cuốn sách "Bản lĩnh blouse trắng"

Sau Tết, tiếp tục giám sát chặt các dịch bệnh
Bé gái 5 tuổi bị mất một bàn tay vì hàng xóm đốt pháo
Tin bài khác
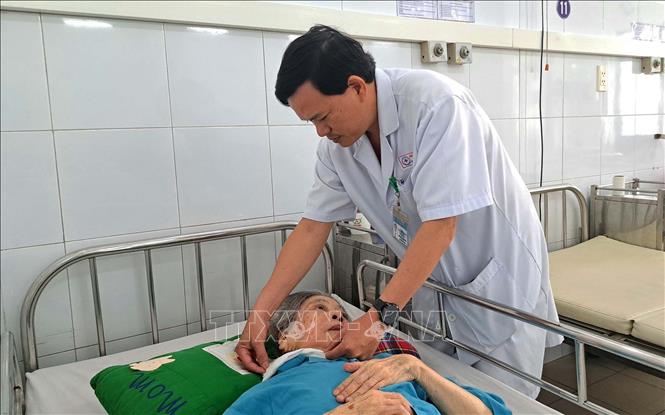
Phẫu thuật loại bỏ khối u "khổng lồ" cho cụ bà gần 90 tuổi
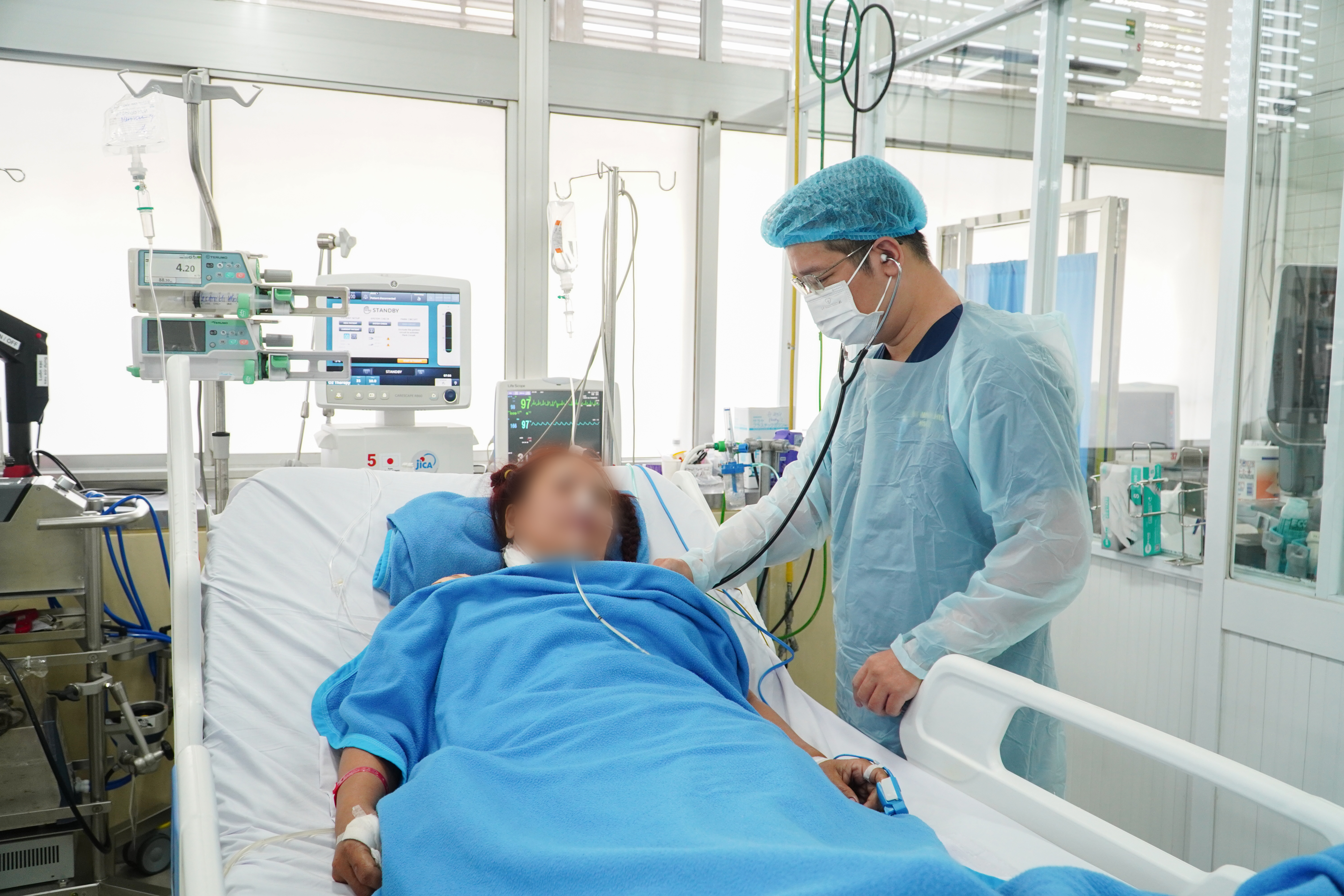
Phối hợp nhiều chuyên khoa cứu sống một phụ nữ bị đâm 17 vết dao

TP Hồ Chí Minh: Em bé đầu tiên được thông tim trong bào thai chào đời khỏe mạnh

Cô gái hôn mê sau phẫu thuật thẩm mỹ đặt túi ngực, hạ gò má

Dập nát bàn tay do nổ pháo tự chế
Đọc nhiều

Cách dịch biển số xe xấu-đẹp tại Việt Nam

Tự soi mình theo Nghị quyết Trung ương 4 để liên hệ, kiểm điểm, khắc phục
![[Megastory] Phát hiện 11 ca nhiễm COVID-19, Thái Nguyên nâng cao các giải pháp ứng phó](https://thainguyentv.vn/stores/news_dataimages/phanletung/112021/02/10/medium/2612_d49d1cca37d4ff8aa6c5.jpg?rt=20211102102614?211102104719)
[Megastory] Phát hiện 11 ca nhiễm COVID-19, Thái Nguyên nâng cao các giải pháp ứng phó

Khu cách ly tập trung đầu tiên trên địa bàn tỉnh Thái Nguyên sẵn sàng hoạt động
Thái Nguyên: 99 ca nghi nhiễm Covid-19, ghi nhận 57 ca mắc Covid-19 (ngày 30/11)
Multimedia
![[Photo] Ấn tượng Khai mạc mùa du lịch Thái Nguyên năm 2025](https://thainguyentv.vn/stores/news_dataimages/2025/042025/27/22/croped/medium/z6545516939579-2461e58882e9442779047235bbba6dd120250427222134.webp?rt=202505061320?250427104257)
[Photo] Ấn tượng Khai mạc mùa du lịch Thái Nguyên năm 2025

"Sau giờ tan ca" - Gắn kết đồng nghiệp, lan tỏa năng lượng tích cực

Khai mạc Giải Đua thuyền truyền thống và Giải Ván chèo đứng Quốc gia năm 2025
![[Photo] Thái Nguyên rực rỡ cờ hoa mừng đại lễ 30/4](https://thainguyentv.vn/stores/news_dataimages/2025/042025/24/16/croped/medium/dji-010720250424163045.webp?rt=202505061320?250424110816)





![[Infographic] - Cảnh báo tình trạng lợi dụng nhóm hỗ trợ “Bình dân học AI” để lừa đảo, trục lợi cá nhân](https://thainguyentv.vn/stores/news_dataimages/2025/052025/04/12/croped/medium/canh-bao-lua-dao-hoc-ai-cuoi20250504120920.webp?rt=202505061320?250504121012)
![[Photo] Người dân Thái Nguyên hướng về ngày Giải phóng miền nam - thống nhất đất nước](https://thainguyentv.vn/stores/news_dataimages/2025/042025/30/23/croped/medium/c8701mp4-snapshot-0004-20250430-16222620250430234944.webp?rt=202505061320?250501112101)
![[Photo] Hội chợ triển lãm 'Công Thương - OCOP Thái Nguyên 2025'](https://thainguyentv.vn/stores/news_dataimages/2025/042025/29/13/croped/medium/z6551526607262-7cce60ef10584ba414b15f63a6aa7ef620250429134405.webp?rt=202505061320?250429085148)
